
R
esumen
A
bstract
25
EFECTO DE MICROORGANISMOS EN LA
CORROSIÓN DE ACERO SAE 1080
Luis-Marcelo Anchaluisa-Parra; Marco-Homero Armendáriz-Puente,
Jhonny-Marcelo Orozco-Ramos
Escuela Superior Politécnica de Chimborazo, Facultad de Mecánica,
Escuela de Ingeniería Industrial.
E-mail: marcelin_9631@hotmail.com
En la industria petrolera, existe una estimación de fallas del 25% al 35% en oleoductos de las insta-
laciones petroleras, que son hidrocarburos favorecidos por microorganismos. Las transferencias de
iones son sustentadas por reacciones químicas, que demuestra el uso de métodos electroquímicos
para su estudio. En la investigación, se analizan muestras de acero con bajo porcentaje de carbono
(SAE 1080), bañadas en un medio rico en cloruros en ausencia y presencia de tres diferentes car-
gas microbianas, en tiempos de exposición de 48 horas y 28 días. Las probetas de acero obtenidas
después del tratamiento a diferentes tiempos de exposición fueron caracterizadas empleando el
análisis de resistencia a la polarización (Rp), espectroscopía de impedancia electroquímica (EIS)
y microscopía electrónica de barrido (MEB). Los resultados mediante Rp y EIS, muestran que el
medio abiótico provoca mayor efecto corrosivo, resultando que los microorganismos tienen un
efecto inhibidor de la corrosión. Los resultados de MEB corroboran los encontrados por Rp y EIS.
Los microorganismos presentan un efecto protector al reducir la velocidad de corrosión y a un
tiempo de exposición de 28 días en ausencia de microorganismos se deteriora considerablemente
la estructura del acero 1080 utilizada durante el desarrollo del trabajo.
Palabras claves: Corrosión microbiológica, acero de bajo carbono, métodos electroquímicos.
In the oil industry, there is an estimated 25 to 35% failures in oil pipelines in oil facilities, which
are hydrocarbons favored by microorganisms. Ion transfers are supported by chemical reactions,
which demonstrate the use of electrochemical methods for their study. In the research, samples
of steel with a low percentage of carbon (SAE 1080) were analyzed, washed in a medium rich in
chlorides in the absence and presence of three different microbial loads, in times of exposure of
48 hours and 28 days. The steel samples obtained after treatment at different exposure times were
characterized using polarization resistance (Rp) analysis, electrochemical impedance spectrosco-
py (EIS) and scanning electron microscopy (SEM). The results by Rp and EIS show that the abiotic
medium causes a greater corrosive effect, resulting in microorganisms having a corrosion inhibi-
ting effect. The results of MEB corroborate those found by Rp and EIS. The microorganisms have a
protective effect by reducing the corrosion rate and at a time of exposure of 28 days in the absence
of microorganisms, the structure of the 1080 steel used during the development of the work is
considerably deteriorated.
Key words: Microbiological corrosion, low carbon steel, electrochemical methods.
Anchaluisa, Armendáriz, Orozco
Fecha de recepción: 26/01/2017
Fecha de aceptación: 15/05/2017

26
INTRODUCCIÓN
Las industrias eléctricas, petroleras, nucleares, del papel y
alimentos, se han visto afectadas por la corrosión micro-
biológica (Videla HA, 2010). Donde existe una estimación
de fallas del 25% a 35% en los oleoductos de las instalacio-
nes petroleras, estas están relacionadas a inconvenientes de
corrosión microbiológica, perturbando la parte interna y
externa de éstas. En la industria, se gastan alrededor de 120
millones de dólares al año en biocidas para contrarrestar
este tipo de corrosión. Estos tratamientos tienen un efecto
malicioso al medio ambiente y a la vida humana además de
ser costosos (Borestein SW, 2012).
Se conoce como biopelìcula al conglomerado microbiano
compuesto por microorganismos como algas, bacterias,
que está formado de una matriz gelatinosa de material po-
limérico extracelular con un elevado contenido de agua
(80 al 95% de la masa) y células microbianas. Esta película
biológica cambia las condiciones de la interfase metal/so-
lución, donde las reacciones que se provocan entre los me-
tabolitos microbianos y la superficie metálica tienen lugar
por dentro o por debajo de la estructura del biofilm.
La bioprotección es la correlación entre los múltiples me-
canismos, metal / biota / electrolito, que producen un efec-
to sinérgico en la inhibición de la corrosión. La inhibición
originada por los microorganismos se debe a la acción
neutralizadora de las sustancias corrosivas presentes en el
ambiente, esto a través de la modificación en la concentra-
ción de oxígeno y del pH del medio, formando películas
protectoras que impiden las reacciones entre el medio co-
rrosivo y la superficie metálica.
MATERIALES Y MÉTODOS
Entre las técnicas electroquímicas utilizadas para el estudio
de la corrosión microbiológica tenemos:
• Potencial a circuito abierto (OCP),
• Resistencia a la polarización lineal (LPR) y
• Espectroscopia de impedancia electroquímica (EIS).
Para el estudio se considera el método potencial a circuito
abierto y Espectroscopia de impedancia electroquímica,
pues son los métodos más utilizados en la industria, debi-
do a que son pruebas electroquímicas sencillas de realizar
y arroja resultados confiables.
Potencial a circuito abierto
Es diferencia de potencial entre el metal
sumergido en un ambiente iónico y un
electrodo de referencia (generalmente un
electrodo de calomel saturado SCE).
La magnitud y signo de este parámetro
depende del metal, de la composición del
medio, temperatura, de las condiciones
hidrodinámicas, pH, etc. En la práctica
resulta ser una prueba muy sencilla de
realizar, una de sus desventajas radica en
que no arroja valores y cambios en velo-
cidades de corrosión.
Espectroscopia de
impedancia electroquímica
Es la aplicación de un voltaje alterno fijo
a un electrodo transformando la frecuen-
cia. Esta técnica establece la existencia de
un monitoreo por transferencia de masa,
además de ser útil en los estudios de pelí-
culas no conductoras o poco conductoras
que recubren metales como las películas
orgánicas. Una de las desventajas es que
los circuitos eléctricos equivalentes son
complicados de modelar, como el caso de
interfaces complejas.
El estudio electroquímico se realiza em-
pleando muestras de acero de bajo carbo-
no SAE 1018 debido a que su utilización
es frecuente, con área de exposición de
1.5 x 1.5 cm, un acabado superficial a es-
pejo. Se emplea un electrodo saturado de
calomel como electrodo de referencia y
una barra de grafito de alta pureza como
electrodo auxiliar.
Además, se utiliza un potencióstato con
interface electrónica a una computadora,
para el registro y procesamiento de datos.
Los electrodos son sumergidos en el me-
dio de cultivo nace a 37 °C previamente
esterilizado por medio de autoclave (20
minutos, 121 °C, 15 psi). La composi-
ción del medio se presenta en la tabla 2.
Los electrodos y termómetro se esterili-
zaron en frío. Los ensayos electroquími-
ISSN 1390-5740 Número 17 Vol. 1 (2017)
ISSN 2477-9105
27
Anchaluisa, Armendáriz, Orozco
cos se realizan con presencia (biótico) y
ausencia (abiótico) de microorganismos,
de signando una celda de trabajo y una
de control, respectivamente. Para el caso
biótico se realizaron conteos microbianos
para la construcción de la curva de creci-
miento microbiano.
Tabla 1. Composición del medio
de cultivo nace
FUENTE: Scielo Analytics
AUTOR(ES): (Treseder, 2014; Martín, 2004)
Para el primer caso se estudió el compor-
tamiento electroquímico cada hora por
periodos de 48 horas y 28 días.
Para el segundo caso se empleó la técnica
de recuento en placa, donde las medicio-
nes fueron hechas los días 1, 2 ,4, 7, 10,15,
22 y 28. Seguidamente se construyeron
las curvas de crecimiento microbiano
para las diferentes bacterias estudiadas y
tiempos de prueba.
Las técnicas electroquímicas aplicadas
son: la estabilización del OCP mediante
su monitoreo durante 55 min. Inmedia-
tamente se efectúa el ensayo de EIS apli-
cando un barrido de frecuencias de 10
5
Hz a 10
–2
Hz, con una amplitud del vol-
taje de 10 mV. Los resultados obtenidos
de impedancia, potencial y densidad de
corriente son analizados para ajustar los
semicírculos y rectas resultantes usando
regresión por mínimos cuadrados y así
poder determinar el valor de la Rtc.
Después de cada ensayo, las muestras son almacenadas en
un aparato para eliminar la humedad llamado desecador,
para posteriormente observar la superficie de éstas en el
microscopio electrónico.
La investigación tiene como objetivo utilizar métodos elec-
troquímicos potenciales a circuito abierto, y espectrosco-
pia de impedancia electroquímica para el estudio del fe-
nómeno de la corrosión microbiológica, utilizando acero
de bajo carbono SAE 1018 expuesto a la operación de dis-
tintas cargas microbianas, con el fin de correlacionar los
diferentes parámetros estudiados.
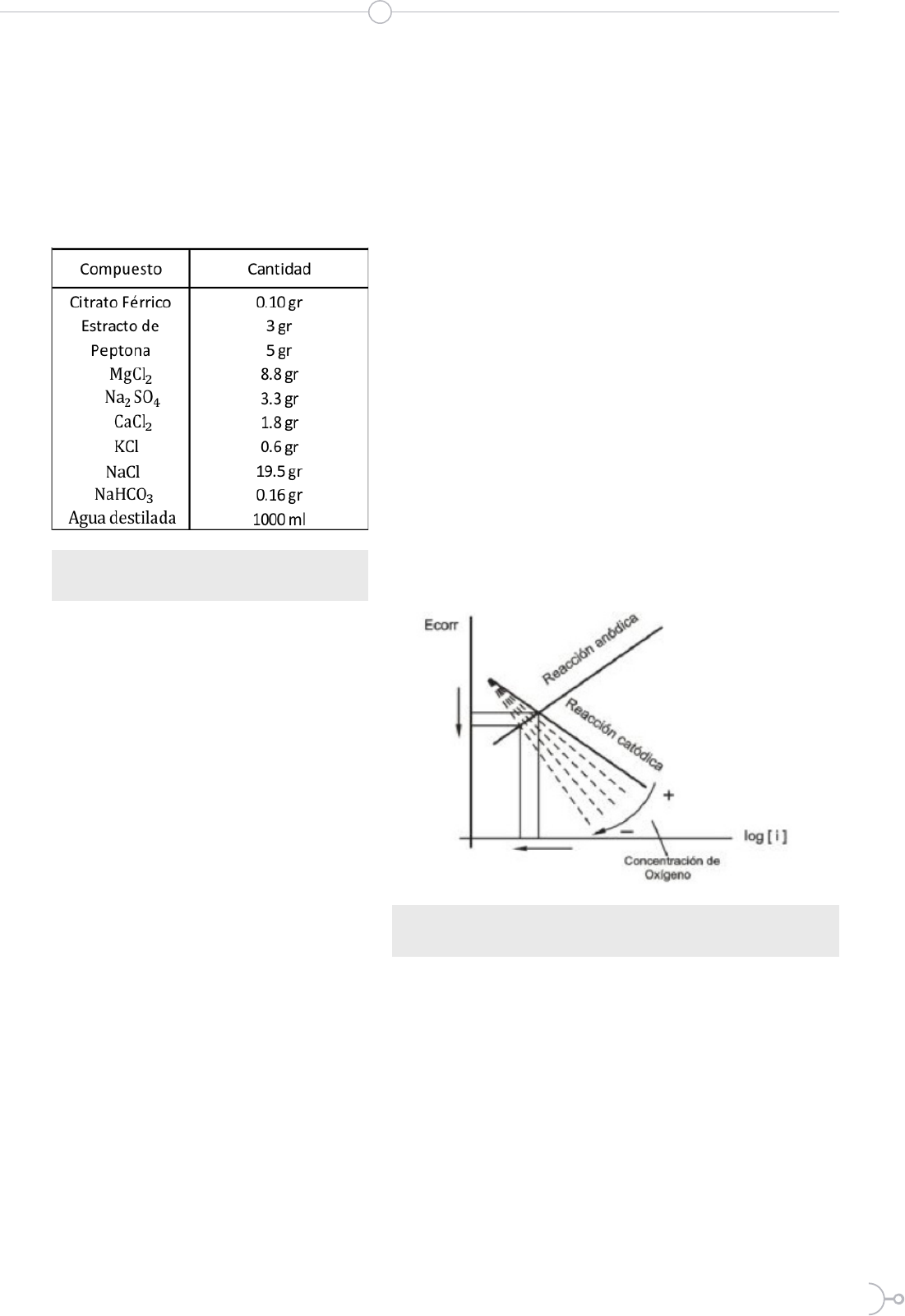
Debido a que los valores de pH están dentro de la zona
neutra, la reacción catódica queda controlada por la re-
ducción del oxígeno. En el diagrama de Evans – Tafel de
la figura 1, se plantea una disminución del oxígeno debido
a la respiración microbiana, lo que ocasiona una polariza-
ción catódica, esto es un cambio dependiente en la recta
catódica que induce una disminución simultánea en los
valores de OCP y Vcorr. Se considera que una disminución
del potencial de corrosión, no necesariamente induce un
aumento en las velocidades de corrosión.
Figura 1. Mecanismo de polarización catódica provocado
por una disminución en la concentración de oxígeno
FUENTE: Scielo Analytics
AUTOR(ES): (Treseder, 2014; Martín, 2004)
RESULTADOS
En las evaluaciones para los ensayos de 48 horas, el cambio
de etapa de retardo a exponencial se muestra aproxima-
damente entre 9 a 10 horas para los dos tratamientos. La
fase estacionaria se alcanza entre los 13 y 15 días durante la
prueba de 30 días, con un alto número de células en el con-
sorcio microbiano, seguido por las bacterias 33 sp. y 25 sp.
28
El consorcio microbiano y bacteria 33 sp. alcanzan la eta-
pa de extinción celular aproximadamente a los 19 días,
mientras que para la bacteria 25 sp. ésta se presenta apro-
ximadamente al día 22.
En la etapa final se presenta en el consorcio microbiano
en un tiempo mucho más corto, debido a la minimiza-
ción de nutrientes en el medio ocasionado por la gran
cantidad de células en la etapa estacionaria con relación a
los demás sistemas bióticos.
De la misma forma, debido a una baja cantidad de célu-
las, la bacteria 25 sp exhibe la etapa de muerte en tiempos
mucho más largos.
OCP 48 horas
Los comportamientos de OCP adquiridos en los tres sis-
temas bióticos experimentan una transformación abrupta
aproximadamente entre 8 y 10 horas de prueba, elevando
hasta valores muy altos y minimizando con altas veloci-
dades hasta alcanzar una velocidad de cambio constante.
La prueba de control presenta una sutil disminución de
OCP sin experimentar cambios abruptos.
OCP 28 días
Las deducciones indican que durante los 7 primeros días
de exposición el consorcio microbiano y bacteria 25 sp
tienen comportamientos iguales y diferentes a los siste-
mas restantes. A partir del día 7, la tendencia de todos
los sistemas es a disminuir con prácticamente una misma
velocidad de cambio.
Los máximos niveles de OCP después del día 7 fueron los
anotados por la prueba de control, y los mínimos los del
consorcio microbiano.
Rtc 48 horas
De la misma manera que los deducciones de OCP, los ni-
veles de Rtc para los sistemas bióticos muestran cambios
abruptos alrededor de 9 a 10 horas de exposición, hasta
alcanzar un nivel en el que se presenta un aumento uni-
forme con respecto a la velocidad para todos los sistemas;
las altas velocidades de corrosión son las producidas por
la prueba de control, escoltadas por la bacteria 25 sp, bac-
teria 33 sp y por último las del consorcio microbiano, lo
que demuestra que el resultado del consorcio microbia-
no en las velocidades de corrosión es baja en cualquier
momento, durante el periodo de tiempo
estudiado; en contra parte, la prueba de
control resulta con las velocidades ma-
yores de corrosión con valores práctica-
mente iguales.
Rtc 28 días
Durante los primeros cuatro días de ex-
posición la actuación de cada uno de los
sistemas es disparejo, en la cual se ob-
serva máximos y mínimos en diferentes
instantes. A partir del día 15 todos los
sistemas tienden a bajar gradualmen-
te hasta que a partir del día 16 tienden
prácticamente a ser los mismos valores
de Rtc. Los experimentos de control
registran las máximas velocidades de
corrosión a partir del día 3; en contra
parte, las mínimas velocidades de co-
rrosión, las anoto el consorcio microbia-
no durante el periodo en estudio, esto
confirma los resultados obtenidos en la
prueba de 48 horas.
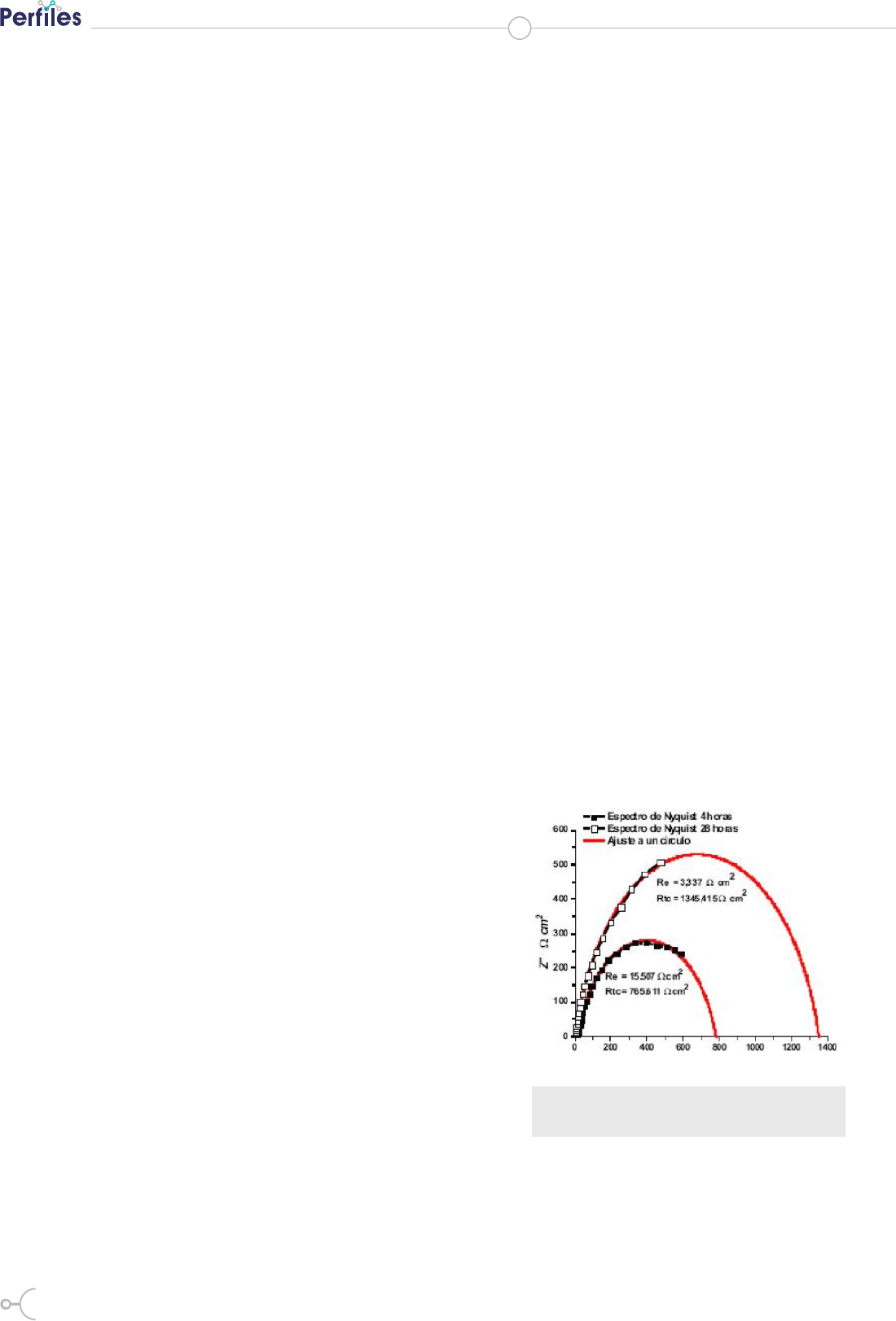
En la siguiente figura se puede observar
los espectros de Nyquist desde la 4 hora
hasta la hora 28 de exposición para las
diversas pruebas de trabajo y control.
Figura 2. Espectros de Nyquist con barridos
de frecuencia de 10
5
hasta 10
-2
Hz.
En ellas se estima que en las frecuencias
asimiladas el control activacional preva-
lece desde el comienzo hasta el final de
los ensayos.
ISSN 1390-5740 Número 17 Vol. 1 (2017)
ISSN 2477-9105

29
Anchaluisa, Armendáriz, Orozco
La extensión microbiana va en aumen-
to en las velocidades de corrosión. Al
mantenerse igual el crecimiento en el
período estacionario, la velocidad de al-
teración de la velocidad de corrosión se
reduce. El aumento o disminución del
OCP indican máximas o mínimas ten-
dencias de corrosión del metal.
La exposición de los cambios rugosos de
Rtc en los ensayos de 48 horas en los sis-
temas bióticos se expone en la siguiente
figura, donde el cambio rugoso de este
parámetro ocurre a la par con el cam-
bio de fase de retardo a exponencial en
la curva de incremento. Los cambios ru-
gosos de OCP y Rtc en los sistemas bióti-
cos, suceden al mismo tiempo, lo que in-
dica que ambos son perjudicados por el
paso de fases en la curva de crecimiento.
Figura 3. Efecto del cambio de fase de retar-
do a exponencial en los valores de (Rtc)
En la figura anterior después de 8 horas
de exposición una desaceleración en las
velocidades de corrosión se relaciona
con una baja velocidad en el OCP. Para
apoyar una posible explicación de esta
relación se presentan en la siguiente ta-
bla donde se observa las mediciones de
pH al inicio y final de cada una de las
pruebas de 48 horas.
FUENTE: Scielo Analytics
AUTOR(ES): (Treseder, 2014; Martín, 2004)
Tabla 2. Valores del pH antes y después de
las pruebas de 48 horas
Los resultados de las pruebas electroquímicos para los
análisis de 30 días son preservados por las observaciones
hechas en el MEB en las probetas del día final para cada
uno de los sistemas estudiados, que se muestran en las
figuras 4 y 6. Al comparar visualmente las imágenes es
notable que el medio de cultivo ocasionó mayores daños
superficiales al material, provocando ataques localizados
en menor densidad, pero mayores en tamaño.
Figura 4. Superficie expuesta al
consorcio microbiano, 800x
Figura 5. Superficie expuesta a la
bacteria 33sp., 800x

30
Figura 6. Superficie expuesta a la
bacteria 25 sp., 800x
Figura 7. Superficie expuesta únicamente al medio
de cultivo, se observan menores
ataques localizados, 800x
DISCUSIÓN
Los daños localizados en las superficies expuestas al me-
dio abiótico fueron debido a la formación de una capa
pasiva en la superficie en los primeros días de exposición,
que conforme aumentó el tiempo de exposición, se rom-
pió el medio de cultivo debido a la alta concentración de
cloruros, provocando la formación y crecimiento de pica-
duras. Estos daños fueron inhibidos en los sistemas con
presencia de bacterias debido a cualquiera de las siguien-
tes posibilidades:
• La presencia de un biofilm protector aisló gradualmente
la superficie del acero con el medio de cultivo conforme
esta capa aumentaba en espesor; sin embargo, la picadura
observada en el MEB en los sistemas bióticos fue causada
por la generación de celdas de concentración provocadas
por la presencia del biofilm.
• Se considera que las velocidades de co-
rrosión son menores en los medios bió-
ticos debido a la continua disminución
de oxigeno ocasionada por el aumento
en número de células, que también dio
lugar a la formación de un biofilm que
ocasiona la formación y crecimiento
gradual de celdas de concentración de
aireación diferencial, logrando simultá-
neamente un efecto de inhibición por
parte de la respiración microbiana y un
efecto corrosivo por parte de la presen-
cia del biofilm. Ambas juegan un papel
de competencia en las velocidades de
corrosión, con un mayor efecto de inhi-
bición antes del día 15, después el cre-
cimiento microbiano deja de influir y
se acentúa el efecto corrosivo debido al
biofilm. Las picaduras observadas en el
medio biótico son debidas a las celdas de
concentración generadas por el biofilm,
siendo menor el efecto de éste en núme-
ro y tamaño de picaduras que en condi-
ciones abioticas.
CONCLUSIONES
• Los microorganismos estudiados com-
pletan en 22 días las cuatro etapas en
una curva de crecimiento.
• El cambio de nivel de retardo a expo-
nencial en la curva de crecimiento afecta
abruptamente el potencial y velocidad
de corrosión en todos los sistemas bióti-
cos estudiados.
• La reducción de la velocidad y poten-
cial de corrosión que experimentan los
sistemas bióticos durante las pruebas de
48 horas, se explica por medio de una
polarización catódica que induce una
disminución simultánea en estos valo-
res.
• Durante los primeros 15 días de expo-
sición, las mayores velocidades de corro-
sión fueron las registradas por el medio
sin bacterias, lo que indica un mayor
efecto corrosivo del medio de cultivo y
ISSN 1390-5740 Número 17 Vol. 1 (2017)
ISSN 2477-9105

R
eferencias
31
Anchaluisa, Armendáriz, Orozco
la acción protectora por parte de los mi-
croorganismos estudiados.
• El efecto corrosivo de las bacterias 25
sp y 33 sp es mayor que la del consorcio
microbiano durante los primeros 15 días
de exposición.
1. Borestein S.W. Microbiologically Influenced Corrosion. Handbook. New York. 2006.
2. Cottis R., Turgoose S. Electrochemical Impedance and Noise. Serie Corrosion Testing Made
Easy. USA. NACE International. 2007.
3. Flemming C. Biofouling in Water Systems (cases) Causes and Countermeasures. Montana, USA.
Appl Microbiol Biotechnol. 2015.
4. Heitz H.E., Flemming C., Sand W. Microbially Influenced Corrosión of Materials. Montana,
USA. Springer 2008.
5. Masfeld F. Polarization Resistence Measurement– Experimental Procedure and Evaluation of
Test Data, in Electrochemical Techniques for Corrosion. Houston. R. Robain Editor. NACE. 204.
2004.
6. Rajasekar A., Maruthamuthu S., Muthukumar N., Mohanan S., Subramanian P., Palaniswamy
N. Bacterial Degradation of Naphtha and its Influence on Corrosion. Corrosion Science 47. 2009.
7. Treseder R.S. NACE Corrosion Engineers Reference Book. Second edition, Houston. NACE
International. 2014.
8. Videla H.A. Manual of Biocorrosión. Florida USA. Lewis Publishers. 2010.
• La técnica electroquímica EIS presenta una buena co-
rrelación en los resultados de Rtc, que enfatiza la efecti-
vidad de ésta, lo cual muestra la conservación de tenden-
cias, así como mínimas diferencias numéricas.